Teoría / Pastas Cerámicas
COMPOSICIÓN Y PROPIEDADES GENERALES DE LAS PASTAS
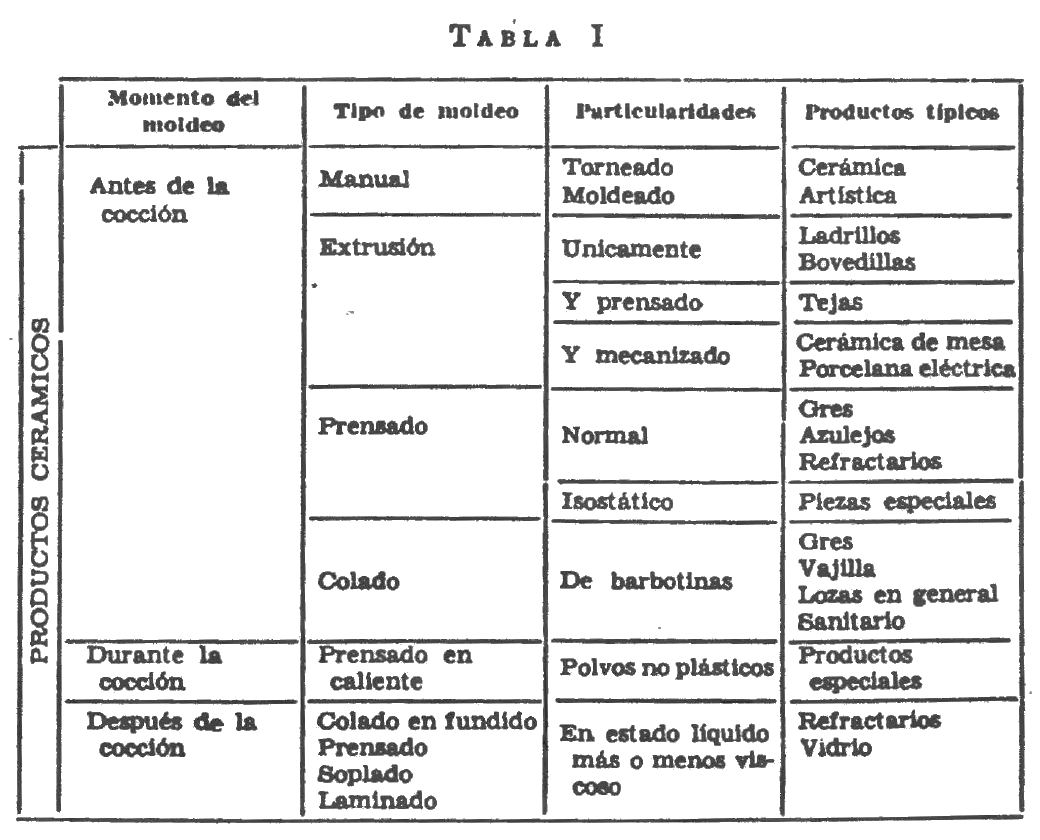
Todos los productos cuyo moldeo se produce antes de la cocción necesitan que sus materias primas se engloben en un todo uno moldeable. Este todo uno es una "pasta". La característica fundamental y común a todas ellas es su comportamiento plástico.
Atendiendo a las características del moldeo pueden definirse dos tipos de proceso: Aquellos en los que las características de la pasta se alteran durante la toma de forma y aquellos en los que no se registra ningún cambio sustancial. El colado de barbotinas pertenece al primer grupo: la succión del molde cambia radicalmente la proporción de agua para dar un cuerpo con una viscosidad mucho más elevada que la de la barbotina. El prensado y la extrusión, dentro de los límites normales, no alteran la proporción de agua en la pasta y pueden clasificarse dentro del segundo grupo. Pero sea como sea el moldeo, e incluso en aquellos procesos en los que no puede definirse claramente un cambio de forma, el comportamiento tanto de la pasta base como del moldeado dependen del comportamiento plástico de la mezcla inicial: de la "Plasticidad".
Los moldeados cerámicos deben su resistencia en crudo a la presencia de la fracción arcillosa y las reacciones durante la cocción se ven altamente favorecidas por el tamaño extremadamente pequeño de las partículas de los materiales plásticos.
En el caso más general, una pasta cerámica tiene dos clases de componentes principales y una serie de aditivos que modifican las propiedades de la pasta acabada, según las exigencias del moldeo. Las dos clases de materia prima son las aportadoras de plasticidad y las fundentes. En algunos casos en los que la fusibilidad requerida no es muy alta y el color del bizcocho no es fundamental, pueden encontrarse tierras arcillosas, que al mismo tiempo que presentan la plasticidad requerida, funden o sinterizan a las temperaturas usadas en el proceso, lo suficiente como para poder servir de materia prima única.
Volviendo al caso más general, las materias primas que aportan plasticidad suelen ser arcillas caoliníticas y caolines elaborados mientras la fusibilidad la aportan minerales del tipo feldespato.
De una manera simplista puede explicarse la sinterización como la cementación de partículas infusibles por un vidrio. De aquí puede deducirse que la cantidad de vidrio formado debe ser suficiente. Como en una composición normal de porcelana el único elemento formador de redes vitrificables es la sílice, es necesaria la presencia de una cantidad mínima de SiO2 en la composición, el déficit relativo en este compuesto de arcillas y feldespato se compensa introduciendo en la fórmula una cantidad determinada de cuarzo.
Las materias primas plásticas no sólo proporcionan las propiedades de moldeo y la estabilidad de las suspensiones, también influyen de modo muy importante en los valores de la resistencia mecánica de las piezas secas, la porosidad tanto en crudo como en cocido e incluso de la resistencia mecánica de las piezas cocidas.
Las materias primas plásticas no sólo proporcionan las propiedades de moldeo y la estabilidad de las suspensiones, también influyen de modo muy importante en los valores de la resistencia mecánica de las piezas secas, la porosidad tanto en crudo como en cocido e incluso de la resistencia mecánica de las piezas cocidas.
La resistencia en seco se ha considerado tradicionalmente como una aportación única de los materiales plásticos. Efectivamente, en una primera consideración se observa que las resistencias en seco individuales de las distintas materias primas varían de 90 a 20 kp/cm² para las arcillas, de 10 a 2 kp/cm² para los caolines y son nulas para los materiales no plásticos ya que no tienen poder auto-aglomerante alguno. Según estos datos la resistencia en seco será mayor cuanto más alta sea la proporción de arcilla en la pasta. Hasta cierto punto esto es verdad, es decir, dada una pasta determinada con componentes plásticos y no plásticos en proporciones significativas ambos, un incremento de plásticos produce un aumento de la resistencia en seco. Del mismo modo el cambio de un componente plástico de baja resistencia por otro de más alta resistencia también produce un incremento del valor de esta variable. En cambio se dan hechos reales como el siguiente: una pasta elaborada con una arcilla de resistencia media 60 kp/cm², y un caolín de 9 kp/cm², da una mezcla de 55 kp/cm² de resistencia media en vez de los 34 kp/cm² esperables.

Si la mezcla incluye sílice en forma de cuarzo molido en proporciones iguales de plásticos y sílice la resistencia obtenida es de 39 kp/cm² en vez de los 27 kp/cm² esperables. Por último si los no plásticos en la mezcla están representados por feldespato y cuarzo de granulometrías similares en proporciones 40/10 la resistencia es de 30 kp/cm².
Todos estos datos y algunos más se han resumido en la tabla III, observándose la particularidad de que las resistencias son siempre más altas de lo que correspondería a una actuación lineal de cada elemento en la mezcla.
En primera aproximación, estos valores más elevados de la resistencia pueden explicarse en función de las compacidades alcanzadas en las probetas que, para un método común de elaboración, es función de la granulometría de la mezcla.
En la figura siguiente se han representado las resistencias a la compresión y las densidades de una mezcla única compactada con energías crecientes: La correlación, aunque no lineal, es evidente.
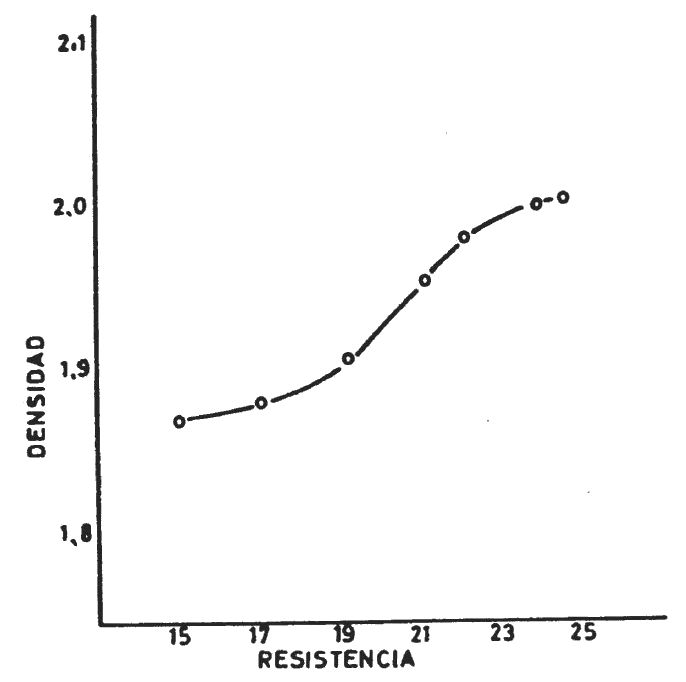
Naturalmente la resistencia mecánica no depende sólo de la compacidad alcanzada, también influye notablemente el poder conglomerante de los componentes, se incrementa la resistencia de un producto conformado a partir de una masa plástica aumentando la cantidad de "plásticos" en presencia. Este efecto puede estudiarse también en la Tabla III comparando las columnas de densidades y resistencias: cuanta más arcilla más resistencia.
Uno de los métodos prácticos de aproximarse a las características ideales requeridas para una pasta cerámica es jugar con la proporción de materiales plásticos y materiales no plásticos en la fórmula.
Esto es posible en las que podríamos llamar fórmulas "completas" en las que figuran al menos un componente de alta plasticidad y otro de baja plasticidad entre los primeros y una materia prima no plástica y fundente y otra no plástica y no fundente; éste es el esquema de una pasta normal compuesta por arcilla, caolín, feldespato y sílice. Un aumento de los no plásticos puede compensarse aumentando la arcilla y disminuyendo el caolín para mantener la plasticidad. La fusibilidad se mantiene jugando con las proporciones relativas de feldespato y cuarzo.
En las pastas de fórmula "completa" la proporción de plásticos/no plásticos se mueve poco alrededor del 50/50, pero una variación del 1% puede ser muy importante por la modificación de granulometría que supone.
ANÁLISIS TÉRMICO DIFERENCIAL
El análisis térmico diferencial nos da mucha información sobre arcillas y pastas cerámicas. Por ejemplo, nos permite diferenciar entre si arcillas en apariencia iguales.
Es bien conocido que las reacciones químicas, o bien, desprenden calor, o bien, lo absorben. Las reacciones que desprenden calor se conocen como exotérmicas. Un caso típico de esta reacción es la oxidación del carbón: C + O2 → CO2 + calor. Las reacciones que requieren calor para ocurrir se llaman endotérmicas. En general, tales reacciones consisten en la descomposición o rotura de una sustancia. Por ejemplo, la descomposición del carbonato de calcio, tan frecuente en los hornos cerámicos: CaCO3 + calor → CaO + CO2. La absorción o desprendimiento de calor en la muestra provocará variaciones de temperatura respecto a su alrededor. Si se requiere calor para una reacción, la temperatura de la muestra disminuirá respecto a su entorno, mientras que si desprende calor, su temperatura aumentará. Estos fenómenos nos permiten determinar las temperaturas a las cuales tiene lugar los cambios o reacciones de la muestra durante la cocción. Por observación de la magnitud de las ganancias o pérdidas de calor y de las temperaturas a las que estas ocurren, es posible diferenciar un mineral de arcilla de otro.
Las partes principales de un aparato para análisis térmico diferencial son un termopar diferencial, el portamuestras, el horno, el registro de los datos y un medio para elevar la temperatura del horno a una velocidad constante.
Un termopar consiste en dos alambres de diferentes metales que cuando se unen por soldadura generan un pequeño pero medible voltaje que es función de la temperatura en la unión de los dos metales. Distintos tipos de cables metálicos pueden utilizarse dependiendo del rango de temperaturas a medir. Los tipos de pares más comunes son los de cobre-constantan, cromo-aluminio y platino con platino más 10% de rodio. Hay tablas estándar que dan los voltajes generados como función de la temperatura.
Un termopar sencillo y un termopar diferencial se ilustran en la figura siguiente. El sencillo mide la temperatura en T1 y el diferencial nos da la diferencia de temperatura entre T1 y T2. Esto constituye la base para las medidas del análisis térmico diferencial.
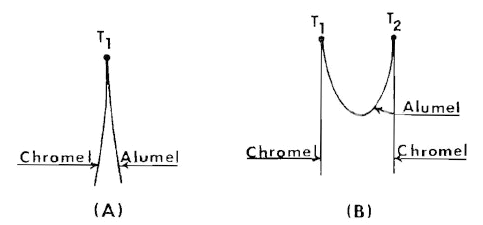
Lo siguiente es una cavidad que contenga la muestra a analizar y sobre la que se coloca una de las puntas del termopar diferencial. La otra se coloca sobre una muestra inerte, es decir, una muestra que no va a sufrir transformaciones durante el calentamiento. Suele utilizarse la alúmina calcinada para este propósito.
Los minerales de arcilla, cuando se calientan, absorben (reacción endotérmica) o desprenden (reacción exotérmica) calor a temperaturas determinadas que son características de cada mineral de arcilla. Cada mineral tiene, por tanto, su propia curva característica de análisis térmico. La figura siguiente muestra dicha curva para caolines, arcillas de bola y bentonitas. Estas curvas presentan ciertas similitudes y diferencias. La curva de análisis térmico diferencial del caolín se caracteriza por dos picos, un pico endotérmico en la región entre 550-650ºC y un pico exotérmico estrecho y bien definido a 980ºC. Si tales picos están presentes, entonces el mineral caolinita está presente en la muestra. Vemos que las primeras cuatro curvas, para los dos caolines y las dos arcillas de bolas, presentan estos picos ya que la caolinita es el principal constituyente. También vemos un pequeño pico endotérmico en la región entre 100-200ºC. Este se debe al calor necesario para eliminar el agua adsorbida en la superficie de las partículas de arcilla. Según se incrementa el área superficial (menor tamaño de partícula) la cantidad de agua adsorbida se incrementará. De hecho, se observa un pequeño efecto endotérmico en los caolines, algo mayor en las arcillas de bola y notablemente mayor en el caso de las bentonitas.

Hay otra diferencia notable entre los caolines y las arcillas de bola. Es el efecto exotérmico de las arcillas de bola en el rango de 300-500ºC. Esto se debe a la oxidación de la materia orgánica presente en la mayoría de arcillas de bola. Esta oxidación del carbón produce calor y la magnitud de este efecto es proporcional a la cantidad de materia orgánica presente. Tal pico en el análisis térmico sirve para indicar que la cocción debe realizarse lentamente y en condiciones oxidantes al alcanzar dicha temperatura de manera que toda la materia orgánica desaparezca al transformarse en dióxido de carbono. Si no ocurre así y los gases se generan posteriormente en la cocción durante la formación del vidrio, pueden aparecer defectos provocados por las burbujas.
Las bentonitas se caracterizan por su gran pico endotérmico en la región de baja temperatura y por dos pequeños picos endotérmicos en regiones, aproximadamente, en 680ºC y 880ºC. En cambio, no aparece el estrecho pico exotérmico de los 1000ºC.
La curva de análisis térmico diferencial nos informa de que algo está sucediendo a una temperatura determinada pero no nos cuenta qué es lo que está sucediendo. Para obtener esta información debemos utilizar otras técnicas, tales como la difracción de rayos X. Estudiando el mineral antes y después de que ocurra algún cambio es posible saber qué es lo que ha ocurrido. A partir de esos datos podemos explicar lo que le sucede a un caolín cuando se calienta. La siguiente información obtenida del trabajo de Brindley y Nakahira explica estos cambios.
Pico endotérmico en 100-200ºC
Es consecuencia del calor requerido para eliminar el agua adsorbida sobre la superficie de las partículas. El tamaño de este pico depende fuertemente del área superficial y de los tipos de iones que pueden asociarse con el agua adsorbida.
Pico endotérmico en 450-600ºC
Según la fórmula química de la caolinita, Al2Si2O5(OH)4, y los esquemas estructurales que vimos, es sabido que la caolinita contiene iones (OH)-. Cuando la caolinita se calienta hasta 450ºC estos iones empiezan a “escaparse” de la estructura en forma de agua según la reacción:
OH- + OH- --> H2O + O2-
2(Al2O3·2SiO2·2H2O) --> 2Al2O3·4SiO2 + 4H2O
Durante este proceso hay una pérdida de peso del 13,95% y un colapso de la red cristalina debido a la reagrupación de los átomos. En esta reorganización, Brindley y Nakahira indican que la cualidad cristalina se pierde a lo largo de uno de los ejes pero no en los otros dos. Con esta transformación a metacaolín el material también pierde sus propiedades plásticas cuando se mezcla con agua. Se sabe que el metacaolín se puede rehidratar sometiéndose a un larga exposición al agua para volver a formar caolinita. De este modo recupera la plasticidad. Durante esta rehidratación podría tener lugar una expansión en correspondencia con la contracción que se observa al perder el agua.
Pico exotérmico a 980ºC
A esta temperatura las capas de metacaolín se condensan para formar un nuevo tipo de estructura llamada “espinela”. Esta tiene aproximadamente la composición 2Al2O3·3SiO en la que se expulsa una molécula de sílice. Es una transformación abrupta.
Pico exotérmico a 1050-1100ºC
Ligeramente por encima del pico exotérmico de 980ºC puede observarse otro pequeño pico. Este es consecuencia de la transformación de la espinela en mullita. Una cantidad adicional de sílice se desprende como cristobalita.
Pico exotérmico a 1200-1400ºC
En este rango de temperaturas hay una formación continua de mullita y cristobalita. La mullita tiene la composición 3Al2O3·2SiO2. Si pretendemos que el cuerpo cerámico contenga poca cristobalita debemos procurar que el tiempo de cocción en este rango de temperaturas sea el mínimo posible.
La serie completa de reacciones y cambios se ilustra en la figura siguiente:
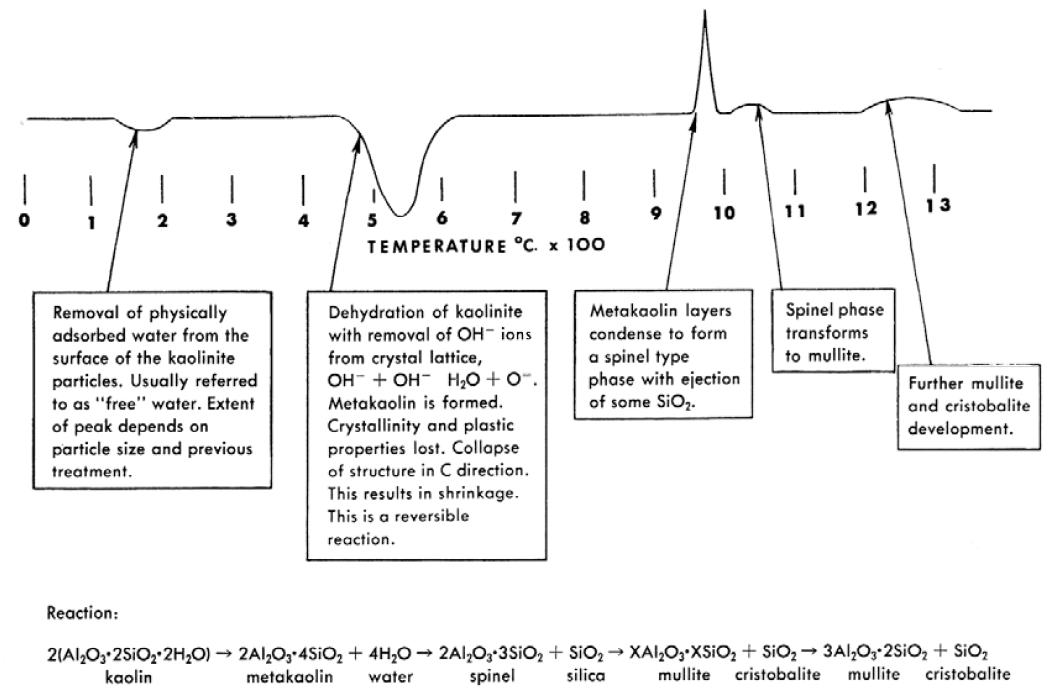
Procesos físicos que tienen lugar al calentar la caolinita
Además de los cambios químicos y estructurales que tienen lugar al calentar el caolín, ocurren otros cambios físicos que tienen también una relación estrecha con la curva de análisis térmico diferencial.
1. Pérdida de peso
Como se discutió previamente, el pico endotérmico en la región de 450-550ºC es el resultado del calor necesario para eliminar el agua química o estructural de la red cristalina. En la caolinita pura esto representa una pérdida de peso del 13,95%. Las curvas de pérdida de peso se representan en la figura siguiente. Tales curvas se han obtenido suspendiendo la muestra en una balanza en el interior del horno, elevando la temperatura del mismo a una velocidad constante y registrando las pérdidas de peso.
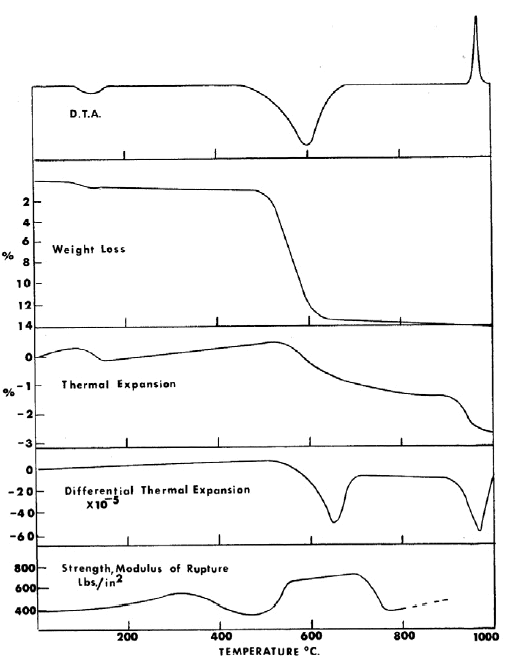
2. Cambios de tamaño
Muchas arcillas encogen al cocerlas. Es importante saber en qué rangos de temperatura la tasa de contracción es máxima. Esto nos permite prevenir tal fenómeno durante la cocción. Siempre que hay cambios, ya sean dilataciones o contracciones, cabe la posibilidad de que el cuerpo cerámico se agriete o alabee. Puede observarse, en el caso del caolín puro de Georgia, que hay una contracción ligera en el rango de los 100-200ºC. Esto se debe a la eliminación del “agua libre”. Alrededor de 500-600ºC hay una contracción mayor correspondiente a la pérdida del agua química cuando la caolinita se transforma en metacaolín. A 950-980ºC ocurre otra súbita contracción cuando el metacaolín se transforma en fase de espinela con la densificación asociada de las especies cristalinas presentes. Si ampliamos la curva a mayores temperaturas, ocurre una rápida contracción a partir de 1200ºC a consecuencia de la formación de una fase vítrea.
3. Resistencia
La figura anterior también muestra la resistencia de un caolín en función de la temperatura. Se observa que la eliminación de los últimos restos de agua adsorbida en torno a 200ºC resulta en un ligero incremento de la resistencia. Un poco por encima de 500ºC, como consecuencia de la transformación a metacaolín, hay un aumento de la resistencia seguido por un decremento a partir de 750ºC
Esos cambios en la resistencia son bastante insignificantes si se comparan con los que se producen en el rango de los 1300ºC. Esta es la temperatura a la cual tiene lugar la formación de vidrio. En la mayoría de los cuerpos cerámicos la formación de fase vítrea es lo que produce la resistencia característica de la cerámica cocida. Por ello, la adición de fundentes de varios tipos para controlar la formación de fase vítrea en el rango deseado de temperaturas es una parte importante en la composición del cuerpo cerámico.
LOS SISTEMAS DE AGUA Y ARCILLA
Dada la importancia de la plasticidad de las pastas cerámicas en cualquier método de conformado, y dado que no hay plasticidad sin el correspondiente porcentaje de agua física, a continuación se va a describir el comportamiento de los sistemas de agua y arcilla.
La molécula de agua
La molécula de agua está formada por un ion oxígeno, O-2, con dos iones hidrógeno, 2H+, formando H2O, una molécula neutra. En la siguiente se ilustra la estructura de esta molécula. Los dos iones hidrógeno no están situados directamente uno frente al otro, sino que existe un ángulo de 104°40' entre ellos. Esta disposición hace que el centro de gravedad de la carga negativa del ion O-2 y el centro de gravedad de la carga positiva de los dos iones H+ estén separados. La molécula de agua, por lo tanto, tiene un lado que actúa como si estuviera cargado positivamente mientras que el lado opuesto tiene una carga negativa. Una molécula así se llama "dipolo". El hecho de que la molécula de agua sea un "dipolo" permite varios tipos de interacciones con otras moléculas e iones que de otro modo no serían posibles.
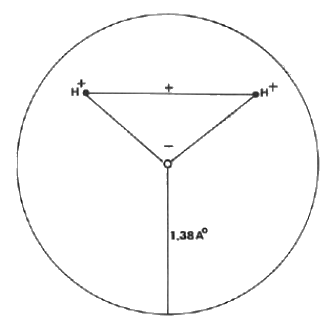
1.- Atracciones dipolo-dipolo
Dado que la molécula de agua actúa como si un lado fuera positivo y el otro negativo y que las cargas disímiles se atraen, dos moléculas de agua pueden asociarse entre sí. Los estudios han demostrado que, por término medio, cada molécula de agua está rodeada por otras cuatro en una disposición tetraédrica. El lado positivo de una molécula se une al lado negativo de la adyacente. Esta disposición puede continuar y dar lugar a la estructura de tipo anillo hexagonal que se muestra en la figura siguiente. Este tipo de líquido se conoce como líquido "polar".
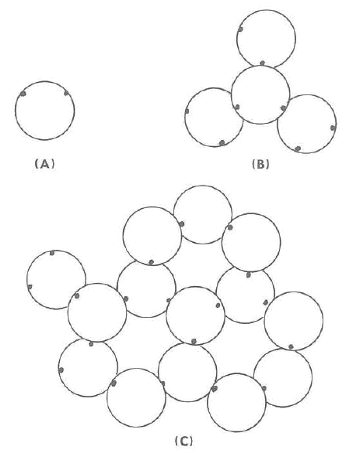
2.- Atracciones ión-dipolo
Es posible que haya atracción no sólo entre las moléculas de agua sino también entre iones y moléculas de agua. Se sabe que un ion en el agua no es una entidad separada sino que está asociado a moléculas de agua y viaja con un cierto número de estos vecinos. El número de vecinos depende del tamaño del ion y de su carga. La figura siguiente, en (A) muestra un ion con carga positiva rodeado por cuatro moléculas de agua no orientadas. Las flechas indican las fuerzas de atracción entre el ion positivo y los lados de las moléculas de agua. (B) muestra los iones asociados con las moléculas de agua y en contacto con ellas. Estas están orientadas con el lado negativo junto al ion y el lado lado positivo lejos del ion positivo.
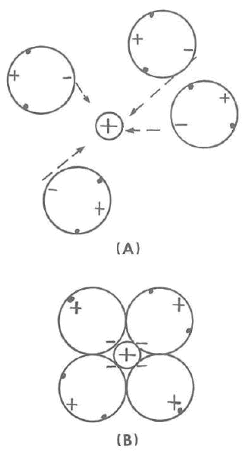
Efecto de los iones en la estructura del agua
Estos conceptos de atracciones dipolo-dipolo e ion-dipolo proporcionan una base para comprender el efecto de los iones en la estructura del agua. Frank y Wen han presentado un modelo sencillo que se muestra en la figura siguiente. En ella vemos las modificaciones estructurales en el agua producidas por un pequeño ion.

Alrededor de un ion esférico de dos a tres angstroms de radio en un líquido como el agua, hay un campo eléctrico de 106 voltios por centímetro. Un campo eléctrico tan intenso ejerce fuertes fuerzas de atracción e inmoviliza las moléculas de agua vecinas más cercanas como resultado de la atracción iondipolo. Esto se muestra en la región (A) de la figura. La región (C) contiene agua normal con la estructura descrita anteriormente como resultado de la atracción dipolo-dipolo. La región (B) tiende un puente entre los dos tipos diferentes de estructura en (A) y (C).
El tamaño de la región (A) puede ampliarse o reducirse cambiando el tamaño o la carga del ion. Los iones pequeños y muy cargados amplían la región de inmovilización (A), mientras que los iones grandes y de carga única la reducen. Numerosos investigadores han estudiado la relación entre las características de los iones y la inmovilización de las moléculas de agua. Los datos indican que el tamaño es un factor importante. Forslind sugiere que los iones pequeños que encajan en la estructura del agua sin perturbarla favorecerían su desarrollo. Los iones más grandes retrasarían su desarrollo. A partir de los datos, el tamaño crítico para el catión monovalente es de aproximadamente 1,36Å de radio. Esto concuerda con el tamaño del "agujero" en la estructura hexagonal del agua que se muestra en la figura de más arriba. Por lo tanto, parece que los iones que caben en este agujero sin romper la estructura mejorarán la formación de esta estructura y la harán más estable, mientras que los iones más grandes que no caben en el agujero rompen la estructura. Este efecto se ilustra en las figuras siguientes.
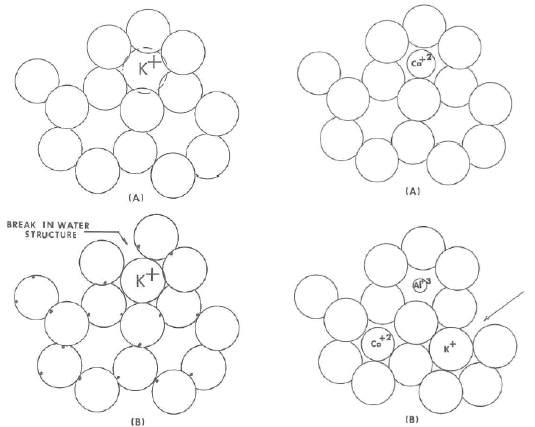
En la figura izquierda, vemos como el gran tamaño del ión K+ rompe la estructura del agua. En cambio, arriba a la derecha se muestra un ion Ca2+ que no distorsiona la estructura.
El concepto de la "capa de agua"
La idea de la inmovilización del agua inducida por iones de carga elevada y tamaño pequeño proporciona una base para el mecanismo de formación de un "manto de agua" o "capa solvatada" alrededor de una partícula de arcilla.
La figura 4-7 ilustra en dos dimensiones la estructura de la caolinita. Si la fractura se produce a lo largo de la línea C-C, se rompen los enlaces. Esto se ilustra en la Figura 4-8. La nueva superficie formada tendrá sitios cristalinos positivos y negativos debido a la exposición de iones Al+3, Si+4, 0-2 y OH-. Es de esperar que estos sitios activos ejerzan una influencia sobre el agua circundante. Esta influencia podría ser incluso más pronunciada que la de un ion individual en solución, ya que estos iones están en la superficie de una red cristalina rígida. Tendrán la capacidad de atraer a la molécula de agua dipolar o a otros iones iones positivos o negativos para satisfacer su deficiencia de carga.
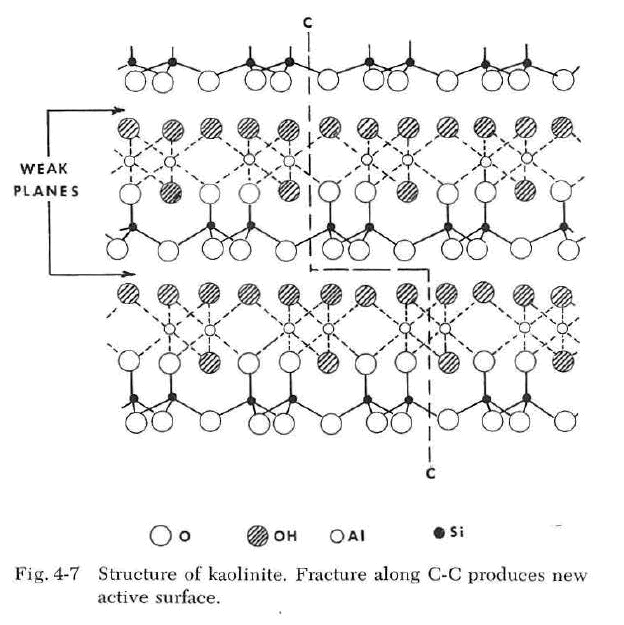
La extensión o el grosor de la capa de agua formada alrededor de la partícula dependerá de los tipos de iones asociados al agua. Los iones que favorecen la estructura del agua como el Ca+2, el Mg+2 y el Al+3 provocarán la formación de una gran capa solvatada. Los grandes iones K+, Rb+, Cs+, NH+4 y Na+ alterarán la estructura del agua y reducirán su tamaño.

La importancia de la estructura del agua en los sistemas arcilla-agua se hará más evidente cuando se analicen propiedades como como la plasticidad y el flujo. En sistemas con partículas de pequeño tamaño y gran superficie, así como con una elevada concentración de sólidos, la distancia de separación entre partículas puede aproximarse al espesor de la película de agua. Las propiedades de esta película de agua ejercen una fuerte influencia en las propiedades de cizallamiento y flujo del sistema arcilla-agua.
Relación entre la red cristalina de la caolinita y la estructura del agua
Para completar el cuadro relativo a la adsorción de moléculas de agua por la superficie de los minerales arcillosos, es necesario discutir la relación que existe entre las estructuras de las dos fases. Si la posición geométrica de los iones y las moléculas es tal que hay un buen ajuste, de modo que no haya un gran grado de desorden en la interfaz, cabría esperar una buena unión y adherencia entre ambos. Como se ha indicado anteriormente, la estructura del agua es de tipo anillo hexagonal, con cada molécula de agua rodeada tetraédricamente por cuatro vecinas. Esta estructura tiene las mismas dimensiones geométricas que los silicatos laminares. El grado de desajuste entre el cristal de caolinita y la estructura del agua es en realidad de sólo -1,1%. Este hecho es probablemente la razón principal por la que los sistemas arcilla-agua exhiben sus inusuales y útiles propiedades.
La figura siguiente ilustra la formación de la estructura del agua en el borde de un cristal de caolinita indicando el buen ajuste entre las dos estructuras y la disposición en anillo hexagonal de las moléculas de agua. La figura más abajo muestra el efecto del ión K+ sobre la estructura del agua. Es obvio que la adición de un ion de este tipo altera la estructura e inhibiría la formación de cualquier estructura a gran distancia. También es obvio que se necesitaría muy poca fuerza para cizallar tal sistema.
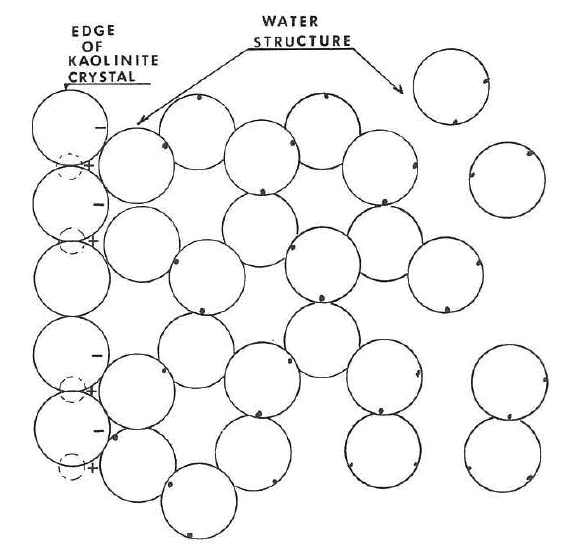
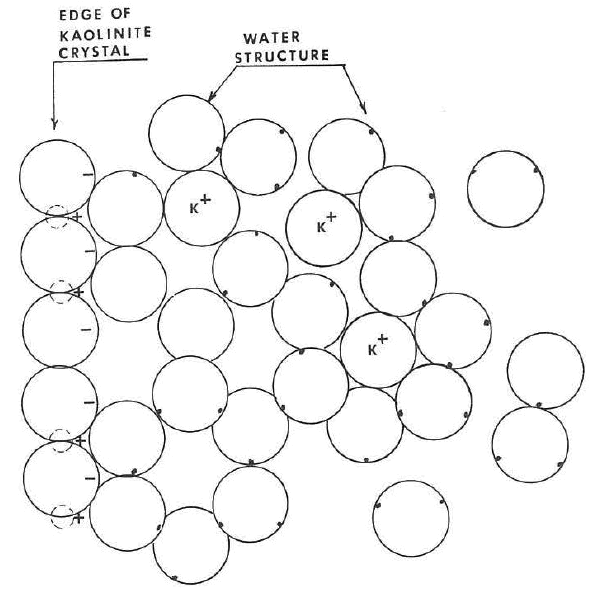
La próxima figura muestra la estructura con el ion Ca+2 encajando en los intersticios de la estructura del agua. La incorporación de un ion de este tipo en esta posición reforzaría enormemente la estructura, aumentaría su acumulación y extensión a grandes distancias desde la superficie del cristal.
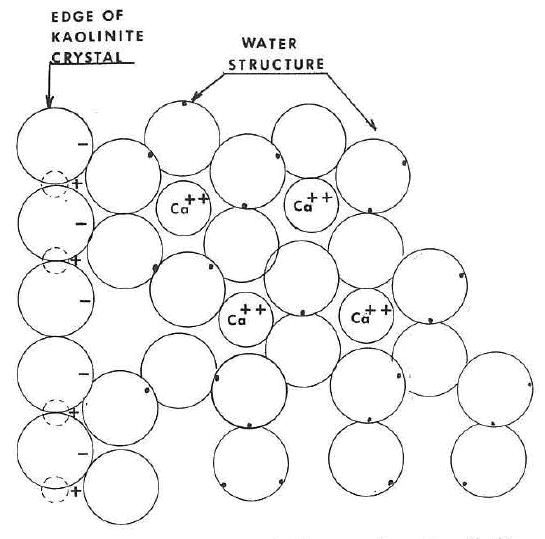
Estos conceptos proporcionan la base para comprender el comportamiento de las barbotinas de colado, así como de los cuerpos plásticos. Los grandes iones monovalentes "rompedores de estructura" se utilizan como defloculantes en barbotinas de colada, ya que se desea una baja viscosidad, un alto contenido en sólidos y un límite elástico bajo o nulo. Por otro lado, aquellos iones más pequeños y multicargados pueden utilizarse para mejorar la plasticidad de las masas arcillosas cuando se desea un límite elástico alto.
BARBOTINAS DE COLADA EN MOLDES
La capacidad de una arcilla para dispersarse en agua mediante la adición de ciertas sustancias químicas conocidas como "defloculantes" sirve de base para la preparación de barbotinas de colada en las que se mezclan arcilla e ingredientes no plásticos, como el sílex y el feldespato. Una barbotina defloculada proporciona una suspensión estable con una viscosidad mínima consistente con el conveniente contenido alto en sólidos. Es el punto de partida necesario para todas las operaciones de colada.
Desarrollo de carga en las partículas de arcilla
La forma en que actúan los defloculantes es la base para comprender el comportamiento de las barbotinas de colada.
Como se ha indicado anteriormente el cristal de caolinita tiene sitios insatisfechos en su superficie. Estos sitios (+) y (- ) tienen la capacidad de de atraer iones o moléculas de cargas opuestas, como vemos en la siguiente figura.
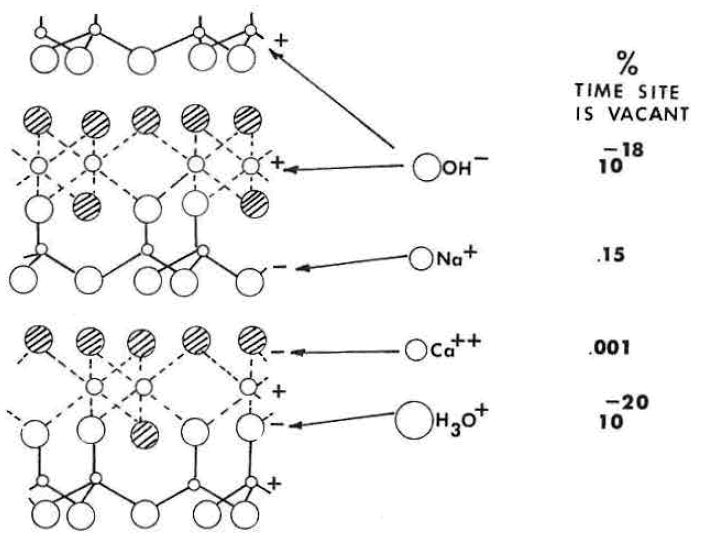
Los porcentajes que aparecen a la derecha indican los tiempos que permanece vacante el sitio del correspondiente ion adsorbido debido a la agitación térmica del sistema.
Si se coloca un cristal de caolinita en agua que contiene hidróxido de sodio, NaOH, el ion Na+ se adsorberá en los sitios (-) y el ión OH- en los sitios (+). Como la superficie del cristal tiene el mismo número de sitios positivos y negativos, se esperaría que la partícula se mantuviera neutra, sin carga total, si cada sitio adsorbiera un ión de carga opuesta. Sin embargo, no es así. Las partículas de arcilla que parecen tener un complemento completo de iones adsorbidos, en realidad presentan una carga negativa. La energía con la que un ion se une a la superficie de un cristal dependerá del tamaño y la carga del ion. Los iones que tienen una carga pequeña se mantendrán menos rígidos que los que tienen una carga alta. Los iones pequeños se mantendrán más unidos a la superficie del cristal que los grandes. La energía térmica mantiene los iones en un estado de movimiento constante. Si la energía térmica es suficiente, puede romper el enlace entre el ion y la superficie del cristal y ese ion puede volver a la solución. Por lo tanto, existe una unión discontinua de los iones a la superficie del cristal; cuanto menor sea la carga y mayor sea el tamaño del ion, mayor será la discontinuidad de la unión. Se puede calcular el porcentaje de tiempo que un ion está unido a la superficie del cristal. En el caso del ion Na+, el cálculo indica que abandona su posición en la superficie cristalina el 0,15% del tiempo. En cambio, el ion OH- permanece en la superficie cristalina un porcentaje mayor del tiempo, abandonando su posición sólo un 10-18% del tiempo. En otras palabras, los sitios negativos del cristal están vacantes durante intervalos más largos que los sitios positivos y el cristal en estas condiciones tiene una carga negativa neta. Las bajas energías de enlace de los grandes cationes monovalentes como K+, Na+, Cs+ y NH+4 dan lugar al desarrollo de una carga negativa en la partícula de caolinita. Los cationes más pequeños y altamente cargados, como Ca+2, Mg+2, Al+3, se mantienen más fuertemente en sus posiciones de adsorción y no se desplazan una vez adsorbidos. En estas condiciones, la superficie no desarrolla una carga neta.
Si todas las partículas de una barbotina de arcilla están cargadas negativamente, se repelerán entre sí, permanecerán separadas y se mantendrán en suspensión durante más tiempo. La barbotina resultante es estable. El aclarado (mezclado con agua) descompone los aglomerados de partículas en partículas individuales, dejando al descubierto nuevas superficies, y permite que el mecanismo de intercambio iónico descrito anteriormente se complete y unifique en toda la barbotina. Este proceso lleva su tiempo, por lo que la viscosidad de la barbotina puede variar en las primeras horas, y es conveniente que el secado y el envejecimiento sean adecuados.
Esta es una de las varias teorías propuestas para explicar cómo se desarrolla la carga en las partículas de arcilla. Las pruebas que apoyan esta teoría son:
- La carga calculada de una partícula basada en esta teoría coincide estrechamente con la carga observada.
- El aumento de la temperatura debe provocar y provoca un aumento en la carga de la partícula. Esto lo confirma Button.
- La teoría predice que se desarrollaría una carga positiva en una partícula de caolinita si se adsorbiera un pequeño catión altamente cargado, como Al+3, y un gran anión cargado individualmente, Cl- o CNS-. Esto también ha sido confirmado por Button.
Los iones capaces de producir una carga en una partícula de arcilla son los mismos que perturban la estructura del agua, mientras que los que producen poca o ninguna carga son los que favorecen la estructura del agua. Estos dos efectos constituyen la base de la floculación y la defloculación.
Cambios de viscosidad
Una de las propiedades más sensibles a la presencia de cationes monovalentes, como el Na+, es la viscosidad. La figura siguiente muestra la viscosidad de una suspensión de caolinita a medida que se añade hidróxido sódico. Se observa que la viscosidad se mantiene en el alto nivel original a medida que se realizan las primeras adiciones de hidróxido sódico y que, en un momento determinado, se produce una disminución brusca de la viscosidad hasta una pequeña fracción del valor original.
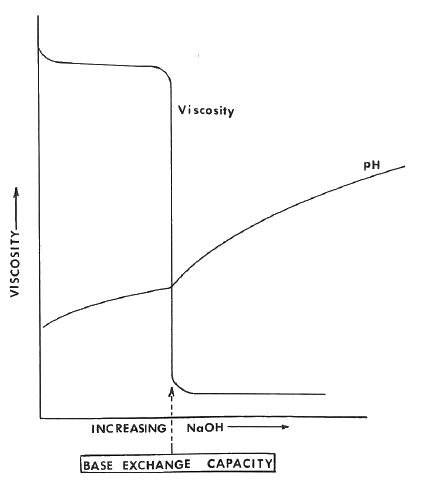
La concentración de iones hidrógeno (pH) indica la concentración de iones H3O+ y OH- en una solución. Una solución ácida tiene un pH bajo y una solución básica un pH alto. La escala de pH va de 1 a 14, siendo neutro un pH de 7. El pH de una suspensión de caolinita pura mostrada en la figura es de 5,5. A medida que se añade hidróxido sódico, el pH aumenta muy ligeramente hasta que se alcanza el mismo punto en el que disminuye la viscosidad. En este punto se produce un aumento repentino del pH que indica que la concentración de iones OH- está aumentando rápidamente en la solución.
Al añadir inicialmente hidróxido de sodio a la suspensión de caolinita y agua, se forman iones Na+ y OH-. Los iones Na+ serán atraídos por los sitios cristalinos (-) y los OH- por los sitios cristalinos (+). Hasta el momento en que se llenan los sitios (+) y (-), esos iones se eliminan de la solución y observamos muy pocos cambios en la viscosidad o el pH. Sin embargo, cuando todos los sitios cristalinos están llenos, nuevas adiciones hacen que la viscosidad disminuya y el pH aumente. Esta cantidad de electrolito añadido se conoce como "capacidad de intercambio" de la arcilla. Más allá de esta cantidad, los iones Na+ y OH- ya no se eliminan de la solución. Los iones Na+ alteran la estructura del agua, la capa de agua rígida ya no es tan gruesa y se observa una caída drástica de la viscosidad. Al mismo tiempo, los iones OH- provocan el aumento del pH.
La "capacidad de intercambio" depende de la distribución del tamaño de las partículas de la arcilla. Esto es de esperar porque los tamaños de partícula pequeños tendrán una mayor área superficial y más sitios cristalinos para ser llenados por los iones adsorbidos.
Aunque se ha hablado del NaOH como defloculante para sistemas de caolinita pura, rara vez funciona en la práctica. Esto se debe al hecho de que la mayoría de las arcillas tienen pequeñas cantidades de sales solubles que contienen calcio. Como se ha indicado anteriormente, el ión Ca+2 es retenido por el cristal de caolinita con mucha más fuerza que el ión Na+. Para sustituir el ion Ca+2 por Na+, el Ca+2 debe ser eliminado del sistema mediante una reacción química que ligará el ion calcio en una sustancia insoluble. La próxima figura muestra la eficacia de tres sales de sodio diferentes como defloculantes para una arcilla contaminada con calcio. En el caso de una adición de NaOH, el ion calcio reaccionaría con el ion hidroxilo para formar hidróxido de calcio: Ca+2 + 2(OH)- → Ca(OH)2. El hidróxido de calcio es ligeramente soluble y, por lo tanto, los iones Ca+2 y OH- se forman de nuevo en la solución. El Ca+2 no se ha eliminado del sistema. En este caso es necesario deflocular con una sal de sodio que contenga un anión que reaccionará con el calcio para formar una sal de calcio insoluble. El silicato de sodio, Na2SiO3, funciona bien en este caso. El ion Ca+2 reacciona con el ion SiO3-2 para formar CaSiO3 insoluble. En la práctica, suelen utilizarse mezclas de carbonato sódico y silicato sódico, fosfato sódico o defloculantes orgánicos.
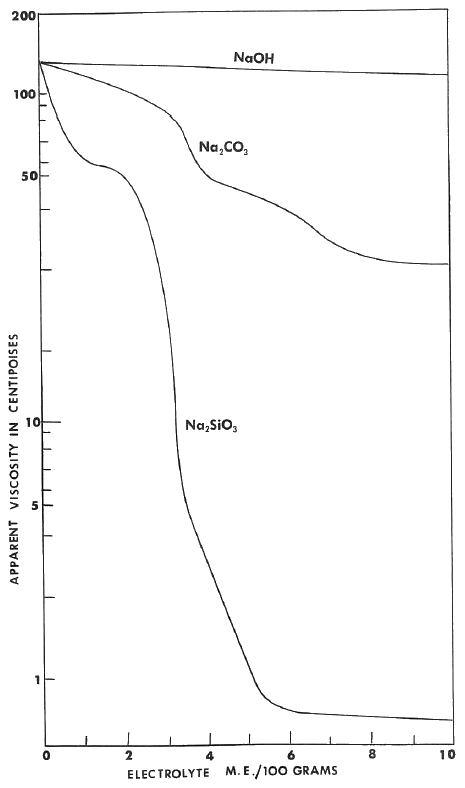
Debido a que los iones defloculantes rompen la estructura del agua y cargan las partículas, un sistema defloculado se comporta de forma totalmente distinta a uno floculado. Así, las partículas se depositan en cada sistema en disposiciones muy diferentes. Se considera que el plano basal (dimensión larga) de un cristal de caolinita tiene una carga negativa muy ligera resultante de la sustitución ocasional de un ion Al+3 en la red por otro que tiene una valencia más baja como Mg+2. A valores altos de pH, por encima del punto de intercambio de bases en la curva de viscosidad o pH, las superficies de los bordes tendrán una carga negativa como se ha explicado anteriormente. La figura siguiente ilustra la distribución de la carga en dos partículas individuales, una en un entorno básico (pH alto) y otra en un entorno ácido (pH bajo). Debido al hecho de que las cargas similares se repelen y las distintas se atraen, se producirán diferentes disposiciones de partículas cuando se produzca la sedimentación o el acercamiento de partículas. Estas disposiciones de las partículas se conocen como "borde con borde" y "cara con cara" o "castillo de naipes" y "baraja de naipes" respectivamente.
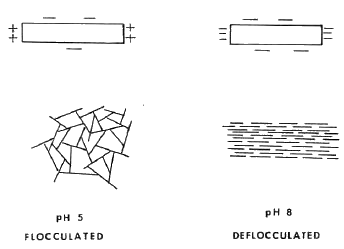
De la imagen se desprende que el sistema defloculado se asentará en una disposición densamente empaquetada. El sistema floculado, en cambio, da lugar a una disposición muy poco compacta con grandes cantidades de agua atrapada entre las partículas. La contracción por secado del sistema defloculado sería mucho menor que la del floculado.
La superioridad de la disposición de "baraja de cartas" en el proceso de colado es una de las razones de la defloculación de las barbotinas. Al retirar el agua, se forma una capa densa y firme junto a la escayola. Los efectos de este tipo de orientación de las partículas se tratarán más adelante.
En resumen, se muestran a continuación algunas de las principales diferencias entre los sistemas floculados y defloculados.

En la elaboración de una buena barbotina intervienen muchos otros factores. Los materiales de partida, el contenido en sales solubles de los materiales, el método de preparación de la barbotina, el control de la defloculación y el control de la gravedad específica de la barbotina desempeñan todos ellos un papel importante. Norton ha dado un excelente tratamiento a este tema (Cerámica fina. Tecnología y aplicaciones. Capítulo 9: Moldeo de la cerámica con pastas líquidas o barbotinas) y se sugiere su lectura.
PRODUCTOS COLADOS EN MOLDES DE ESCAYOLA
El proceso más complicado es el de colado. No solamente se produce un secado sin retracción (mientras la pieza está en el molde) como en el prensado, o una conjunción de tres fases de secado como en los productos extruidos con alta humedad, sino que la conformación de la pieza producida por la energía de succión del molde es en sí un proceso mucho más complicado, que da como resultado inicial un moldeado con un elevado contenido en agua, por encima del 30%, y con una textura no uniforme.
Las peculiares condiciones del moldeo por colado se han esquematizado en la figura siguiente.
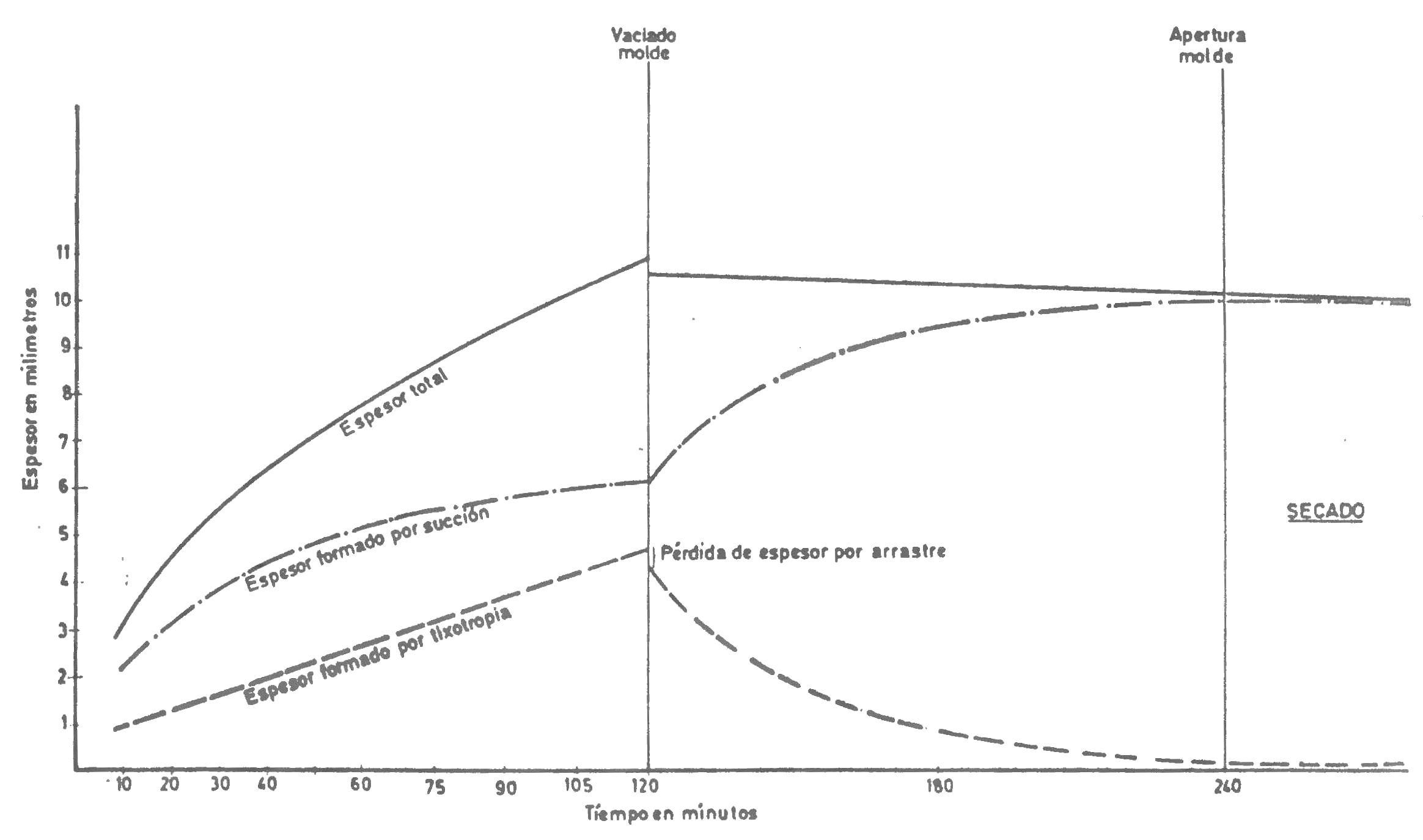
En el momento de entrar en contacto barbotina y molde se produce una succión por parte de éste que da lugar a un depósito de materia sólida con más o menos agua ocluida. La velocidad de formación de este depósito decrece con el tiempo, pues él mismo se opone a la penetración del agua en el molde. En la figura este mecanismo corresponde a la línea de trazos y puntos.
Al mismo tiempo, debido al aumento de densidad en las inmediaciones de la pared formada y posiblemente a una emigración de iones SO4 floculantes, desde el molde hacia la barbotina, y favorecido el fenómeno por el estado de reposo, se produce una estructura tixotrópica que crece también con el tiempo de colada. En la figura este mecanismo se ha representado con línea de trazos.
El espesor total sigue aproximadamente una ley de formación E = K · √t . Si se toma t en minutos, K suele tener valores comprendidos entre 1 y 2.
En la figura la suma de los fenómenos que ocurren durante el colado se ha representado en forma de linea continua.
El espesor formado por cada mecanismo depende de las características de la barbotina y la preponderancia de uno u otro está relacionada con el método y la intensidad de la defloculación.
No puede decirse que sea más favorable el colado de barbotinas de baja tixotropía, que lógicamente forman casi todo el espesor por el mecanismo que hemos llamado "de succión". El vaciado de los moldes se produce ciertamente con mayor facilidad pero, en general, los espesores totales formados son inferiores y las características de secado de los colados obtenidos -"demasiado secos"- pueden dar lugar a pérdidas importantes que no se muestran más que como grietas de cocción, sobre todo en piezas grandes o de formas complicadas.
En un momento determinado, marcado en la figura, para 120 minutos, con una línea vertical, se produce el vaciado del molde. La formación de estructura tixotrópica no sólo se detiene sino que una parte de ella se destruye en el acto por arrastre. Este fenómeno está indicado en forma de escalón brusco en las líneas que representan, en dicha figura, el espesor total formado y el espesor de estructura tixotrópica.
Como la succión del molde continúa en tanto se mantiene el contacto de la pieza con él, el espesor formado por tixotropía evoluciona perdiendo agua, hacia la forma "de succión". Esta segunda fase del proceso de colado recibe normalmente el nombre de "tirado". En ella se produce una contracción difícil de medir, que en cierto sentido es una contracción de secado. Este fenómeno también está representado en la figura: el "espesor tixotrópico" va desapareciendo cada vez más lentamente y el "espesor de succión" va aumentando del mismo modo. Al mismo tiempo se produce una pérdida del espesor total debido a la aproximación entre partículas sólidas que se produce durante el fenómeno descrito.
Durante el "tirado" se incrementa la resistencia mecánica de la pieza. Cuando ésta alcanza un valor suficiente el molde se abre y la pieza se extrae en una secuencia más o menos rápida.
El tiempo de tirado se determina empíricamente y pueden producirse problemas si no es el apropiado: Si es corto dará piezas con menos resistencia de la necesaria, o si es demasiado largo, dará piezas agrietadas por contracciones impedidas por el molde.
Una vez fuera del molde sigue un proceso de secado normal con una fase de pérdida de agua acompañada de contracción y otra con pérdida de agua sin cambios de volumen, según los mecanismos normales.
Es una experiencia común en las fábricas que trabajan por colado que las barbotinas más defloculadas necesitan más tiempo de permanencia en el molde. La velocidad con que se forma "pared" es menor cuanto mayor es la cantidad de defloculante utilizado.
Todos estos efectos pueden explicarse por la estabilización de las pastas producida por la defloculación, que hace más lento el proceso de "deshidratación" de la barbotina y que precisamente esta lentitud del proceso permite un mejor acomodo de las partículas que crea una estructura más resistente y con menos agua ocluida.
En todo lo explicado sobre el colado de barbotinas se ha supuesto que el molde de yeso era ideal. Todos los efectos y defectos atribuibles a unas propiedades inadecuadas de la barbotina pueden atribuirse y proceder de un molde de yeso incorrecto.
Los moldes de yeso muy duro tienen una porosidad muy baja. La succión del agua es muy lenta y pueden dar lugar a bajas velocidades de formación de pared. Los colados aunque finos no presentan apenas estructura tixotrópica, los interiores quedan limpios y sin escurriduras.
Cuando el yeso es blando, su porosidad es alta. La succión ejercida sobre el agua de la barbotina es muy violenta; lo normal en este tipo de moldes es que se formen espesores grandes con una preponderancia de la estructura tixotrópica.
Naturalmente el resultado del colado depende de igual modo de las propiedades de la barbotina y del molde. No se pueden establecer las características ideales de una ignorando al otro. La mejora de los resultados de una producción debe realizarse forzosamente trabajando en ambos campos.
Una barbotina sobredefloculada, sin tixotropía, con una baja velocidad de formación de pared irá mejor con moldes blandos. Una barbotina muy tixotrópica irá mejor con moldes poco porosos. Todos estos fenómenos se han resumido en la tabla VIII.

Como los moldes sufren un desgaste mecánico importante por choques, roces, limpiezas, etc, la tendencia normal es a hacerlos más duros, entre otras cosas porque las operaciones de pulido de una pieza colada en un molde con poco desgaste son muy inferiores a las necesarias en una pieza colada en un molde viejo o desgastado.
Los moldes de yeso duro tienen además la ventaja de que pueden realizarse con paredes más finas. La disminución de peso en los moldes es una importante mejora en cualquier proceso industrial, pero no la única. Los moldes de pared más fina se recuperan mejor, es decir, pierden antes el agua absorbida durante el colado ya que la cantidad total de agua almacenada es inferior y el gradiente de humedades en el interior de la pared más acusado.
La dureza del molde está relacionada con la proporción yeso-agua utilizable. La dureza superficial va acompañada por otras propiedades, y así a menor agua de amasado son superiores todas las resistencias de tipo mecánico y la densidad, e inferior la absorción de agua.
El yeso utilizado en la industria cerámica es el llamado hemihidrato, cuya fórmula química corresponde a SiO4Ca· ½H20 que a su vez se presenta en dos formas cristalinas, una de mayor energía interna llamada hemihidrato β y otra más estable, mejor cristalizada, llamada hemihidrato α.
Desde el punto de vista de los moldes para cerámica la diferencia más importante entre ambas clases de hemihidrato está en la cantidad de agua necesaria para conseguir una consistencia apropiada en la masa. Mientras los yesos fundamentalmente compuestos de hemihidrato β necesitan de 80 a 90 ml de agua por cada 100 g de yeso, los ricos en hemihidrato α pueden amasarse con 30 ó 40 ml de agua por 100 g de yeso, e incluso se producen yesos especiales trabajables con 23 ó 25 ml.
Si se piensa que la reacción química de fraguado: SiO4Ca·½H2O + H2O → SiO4Ca· 2H40 no consume más allá de 18,6 g de agua por 100 g de yeso y que el resto del agua sobrante debe eliminarse en el secado posterior del molde dejando un volumen de poros igual a su propio volumen, pueden explicarse todos los fenómenos anteriormente descritos.
En la cerámica colada debe jugarse con la proporción de ambos hemihidratos de forma que se obtengan moldes de una resistencia suficiente con una porosidad también suficiente. Normalmente, y sin más valor que el de una orientación, suelen utilizarse yesos que den una consistencia de trabajo buena con 60 ó 70 ml de agua por 100 g de yeso.
EFECTOS DE ORIENTACIÓN DE LAS PARTÍCULAS
Dado que las partículas de la mayoría de los minerales arcillosos tienen forma de placa, cabe esperar que se orienten durante cualquier operación de conformado. Esto se muestra para una partícula individual en la figura siguiente. Los resultados son los mismos independientemente de los medios que se utilicen para aplicar la fuerza externa
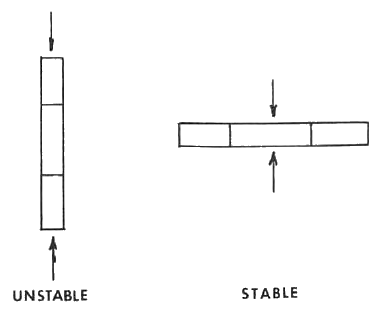
Antes de discutir los diversos defectos individuales que pueden ser causados por la orientación de las partículas, repasemos el trabajo de Williamson sobre los efectos de la orientación en la contracción.
Contracción diferencial causada por efectos de orientación
La contracción diferencial puede demostrarse de forma sencilla con el siguiente experimento. Un bloque de arcilla en forma de cuña se aplana progresivamente extendiéndolo con un rodillo, como en la elaboración de la masa para tartas. Otro método sencillo consiste en dejar caer repetidamente el trozo de arcilla sobre una superficie plana, dándole la vuelta cada vez para que las superficies opuestas reciban el mismo impacto. A continuación, se corta una pieza de prueba y se mide la contracción en las direcciones perpendicular y paralela al plano de laminación o impacto. Como consecuencia del laminado o del impacto, las partículas de arcilla cercanas a la superficie se orientan de la manera indicada en la figura de abajo. La contracción se mide en las direcciones perpendicular y paralela al plano de laminado o de impacto. La medición de la contracción en dos direcciones da los resultados que se muestran en la tabla siguiente.
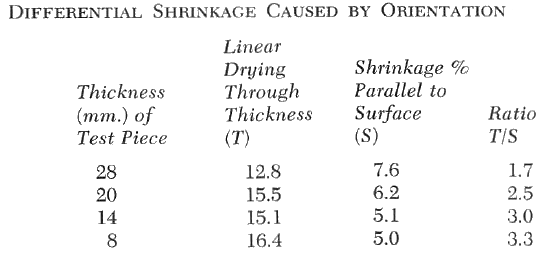
La relación entre la contracción del espesor y la contracción de la superficie aumenta a medida que la pieza es más fina. Esto se debe a que un mayor porcentaje de las partículas está orientado. La contracción es mayor en la dirección perpendicular a la orientación de las partículas porque en esta dirección hay más películas de agua por unidad de distancia.
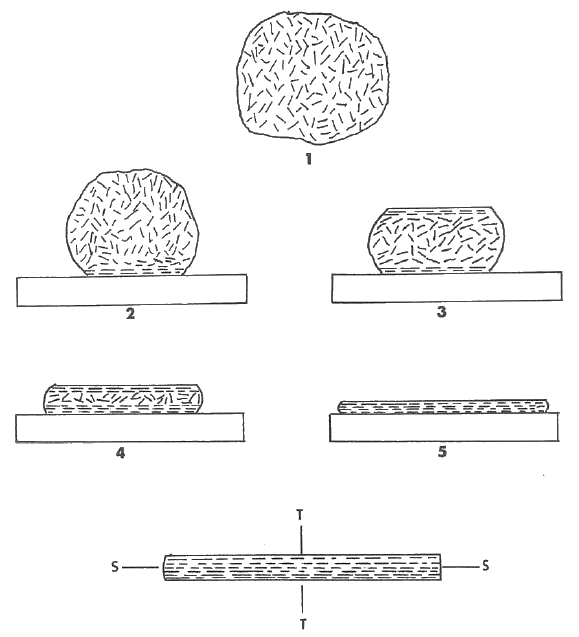
Si la relación grosor-diámetro de una partícula de caolinita es de 10 a 1, cabría esperar una diferencia teórica en la contracción de 10 a 1. La orientación completa de las partículas nunca se alcanza y en el experimento muestra una relación de 3,3 a 1. Esta diferencia es, no obstante, significativa y lo suficientemente grande como para dar lugar a problemas de secado y cocción.
Esta diferencia en la contracción por secado causada por la orientación de las partículas puede representarse en la conocida curva de contracción de secado que se muestra en la figura siguiente.
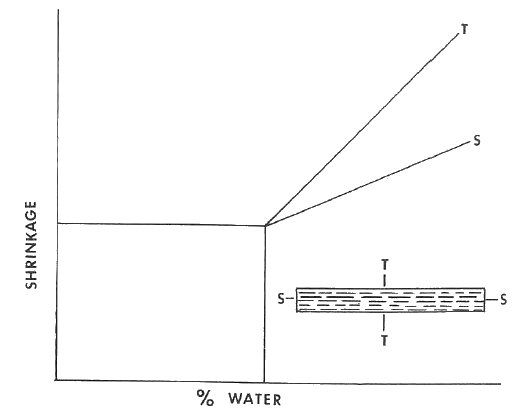
Barbotinas de colada
La eliminación del agua de una barbotina de colada por un molde de escayola da lugar a la orientación de las partículas de arcilla en forma de placa con su dimensión larga paralela a la superficie del molde. En una esquina aguda, como se muestra en la figura siguiente, habrá un cambio repentino en la orientación de las partículas entre la pared lateral y el fondo. La pared lateral y el fondo tendrán sus direcciones de contracción máxima perpendiculares entre sí y la pieza tenderá a agrietarse durante el secado en el punto indicado.

El remedio es hacer esquinas más redondeadas para que el cambio en la dirección de orientación no sea tan brusco y las tensiones resultantes se distribuyan a lo largo de una distancia mayor.
Extrusión
Weymouth y Williamson han demostrado que cuando una arcilla es forzada a atravesar un troquel, la arcilla próxima al troquel queda rezagada con respecto al centro de la columna extruida. Esto se debe a la fricción en la interfaz arcilla-matriz. Esto hace que la columna extruida tenga un alto grado de orientación de las partículas paralela a esta superficie, como se muestra en la figura siguiente.
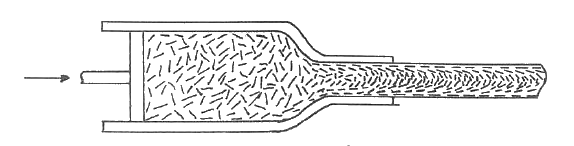
Uno de los resultados, en casos extremos, es el desprendimiento de la capa superficial. La capa superficial se encogerá menos en la dirección de extrusión que la interior. Por lo tanto, estará sometida a compresión. Un choque mecánico posterior puede provocar el desprendimiento de dicha capa superficial. Esto es similar al fallo por compresión de un esmalte (shivering).
Orientación causada por el torno alfarero
Aunque las fuerzas empleadas en el conformado manual de piezas en un torno de alfarero son pequeñas, se produce una orientación de las partículas. Al "levantar" una pared vertical, los dedos ejercen presión en ambos lados de la pared. Las partículas de las superficies son móviles como resultado de la adición de agua utilizada como lubricante. Las partículas se orientan con sus dimensiones largas perpendiculares a la presión. Del mismo modo, cuando se moldea el fondo de la olla, la fuerza se ejerce en dirección descendente o perpendicular a la de la pared lateral. Esto provoca que la dirección de orientación de las partículas del fondo sea perpendicular a la de la pared lateral y que la contracción entre el fondo y la pared lateral sea diferente. Por lo tanto, es probable que se produzca una grieta en la esquina inferior, que es la unión entre las dos direcciones de orientación. La tapa de un cacharro se contrae más a lo largo de su diámetro que el borde. La contracción del borde se distribuye a lo largo de su circunferencia, lo que traducido a la contracción diametral es mucho menor. Este hecho debe tenerse en cuenta para asegurar un buen ajuste entre la tapa y el borde.
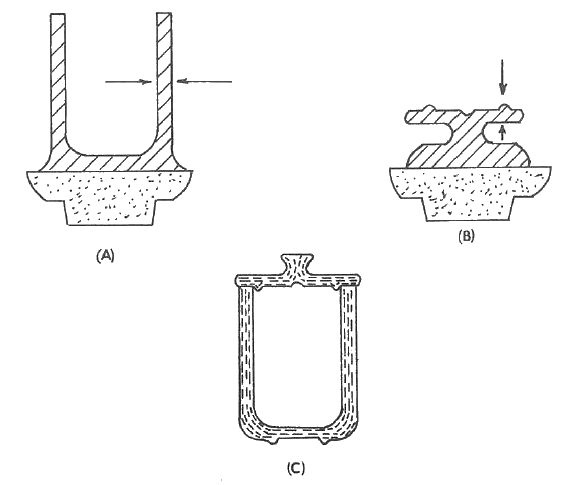
El efecto del amasado
La arcilla plástica suele prepararse a partir de una lechada de arcilla y agua de la que se elimina una parte del agua, ya sea por prensado con filtro o vertiendo la lechada en tinas de yeso donde el agua se elimina por absorción. Cualquiera de los dos métodos da lugar a un alto grado de orientación de las partículas en forma de "baraja de cartas". También se produce una distribución no uniforme de la humedad en las tortas resultantes. Si no se toman medidas para minimizar estos dos efectos, sería difícil fabricar una pieza libre de defectos derivados de la contracción diferencial.
El amasado sirve para aleatorizar la disposición de las partículas y distribuir la humedad de manera más uniforme en toda la masa. En el proceso de amasado, generalmente se utiliza un alambre de pequeño diámetro para cortar la masa plástica, ya que este método produce un efecto mínimo de orientación en las superficies cortadas. Las porciones se lanzan juntas y el proceso se repite una y otra vez. Aunque la distribución completa al azar de la orientación nunca se logra, y siempre habrá una orientación localizada presente, un amasado adecuado la minimiza hasta el punto en que no tiene consecuencias. Otras funciones del amasado incluyen la eliminación gradual del exceso de agua y de las burbujas de aire.
Contracciones diferenciales por cocción
Cox y Williamson han demostrado que las piezas que muestran contracción diferencial durante el secado también muestran contracción diferencial durante la cocción. La contracción durante la cocción también es mayor en la dirección perpendicular a las láminas de arcilla secas. Esto se debe al hecho de que cuando se elimina el agua químicamente combinada de la estructura de la caolinita, como se discute en un tema anterior, la estructura colapsa en la dirección perpendicular a la superficie de la lámina, pero conserva su estructura en la otra dirección.
Uno de los efectos de la contracción durante la cocción es el desarrollo de juntas, especialmente en las piezas moldeadas por colada. A pesar de que las partes del molde encajen estrechamente, las juntas serán visibles después de la cocción. Esto es cierto incluso si se raspan o cortan después del secado. Este efecto se ilustra en la figura siguiente.

En (A) la pieza está en el molde, en (B) ya ha salido del molde, en (C) se han repasado las juntas, y en (D) la pieza está cocida.
Norton proporciona tres métodos para corregir este defecto.
- Golpear ligeramente la junta con un martillo, causando un flujo plástico y rompiendo la orientación de las partículas en la junta.
- Hacer una cocción de bizcocho a una temperatura ligeramente inferior a la temperatura de maduración y eliminar la junta utilizando una rueda de esmeril. Volver a cocer para alcanzar la madurez.
- Cortar una ranura desde la superficie de la junta y volver a llenarla con arcilla plástica.
Es imposible producir una arcilla plástica libre de orientación de partículas. Esta orientación es mayor en sistemas que están defloculados, como en las barbotinas para colado. Esto se debe a la mayor movilidad de las partículas, así como a la distribución de carga en las partículas en tales sistemas. A menor tamaño de partícula, la arcilla es más susceptible a los efectos de orientación. Materiales de grano grueso como chamota, pedernal y feldespato tienden a disminuir tales efectos.
Aunque estos efectos no siempre son problemáticos para el ceramista, y aunque ciertas prácticas tradicionales pueden ayudar a mantenerlos bajo control, se debe reconocer las consecuencias de la orientación de partículas.
PRODUCTOS FINALES
Hay dos momentos críticos en la producción de cerámica en los que la formulación de las pastas influye de forma muy notable. El primero es el secado. El segundo es la primera fase de la cocción.
Durante el secado de las piezas moldeadas en húmedo se producen unos cambios dimensionales de una magnitud suficiente como para producir una nucleación de grietas si se dan contracciones diferenciales importantes. De aquí la importancia de realizar un secado cuidadoso.
Supongamos una bola de materia plástica como la de la figura 6 a continuación, que se seca; si la velocidad de emigración del agua de la superficie al medio ambiente "V'' es mayor que la de emigración del núcleo húmedo a la superficie "v", se creará una capa exterior más seca, que ha contraÍdo más, y que se encontrará sometida a tensiones que deforman esta superficie mientras está en estado plástico y que causan grietas cuando, en estado rígido, se supera la resistencia mecánica del material.
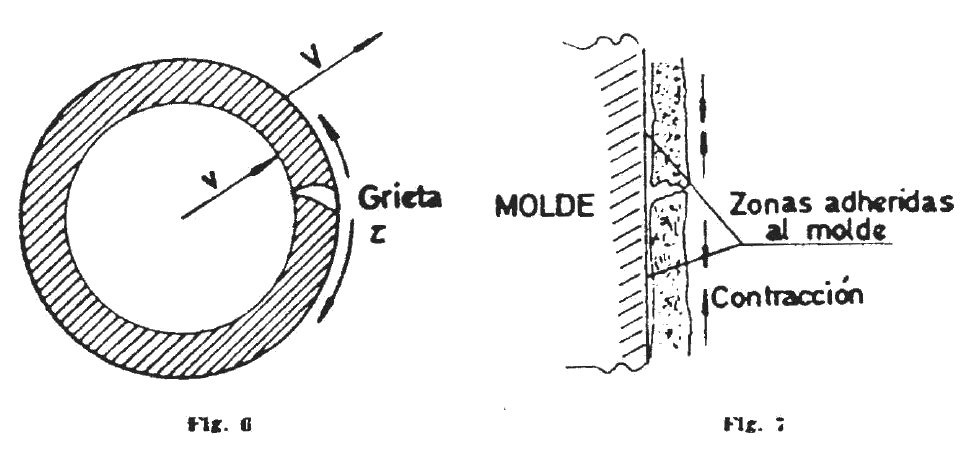
De aquí la importancia de utilizar pastas que tengan contracciones de secado bajas y resistencias altas en seco.
En el caso de los productos colados, que en general son huecos y cuya parte interior permanece plástica durante mucho más tiempo que la exterior, el mecanismo de formación o nucleación de grietas es distinto. Aquí las tensiones se crean por adherencia al molde de yeso. Si la contracción es lenta, como ocurre cuando la aportación de agua del interior a la superficie es importante, o de otro modo, cuando el interior tiene un espesor suficiente formado por tixotropía, se desprende la pieza del molde antes de que se supere su resistencia mecánica, o bien la contracción general de la pieza se produce cuando la superficie tiene una plasticidad residual suficiente como para admitir aún ligeras deformaciones; en estos casos no se producen grietas.
Cuando las pastas son poco plásticas o por otras circunstancias, como una defloculación exagerada o un contenido demasiado alto de coloides orgánicos, se produce un endurecimiento muy rápido de la pared tirada, la contracción de secado puede dar lugar a la formación de microfisuras que en su mayoría se sueldan en procesos posteriores, pero aquellas que no lo hacen producen un incremento notable del número de roturas durante la cocción. Este fenómeno se ha esquematizado en la figura 7.
Durante las primeras fases de la cocción de la mayor parte de la cerámica industrial, es decir, por debajo de los 550-600ºC se pierde una parte importantísima de la resistencia mecánica en seco y, al mismo tiempo, la combustión de las materias orgánicas y la deshidratación de los minerales arcillosos provocan los mayores cambios físicos en la naturaleza de la pieza. En este momento se produce otra nucleación de grietas y el crecimiento de las nucleadas durante el secado. Si el calentamiento ha sido muy rápido y las diferencias de temperatura entre partes de la misma pieza son importantes, se generan grandes tensiones que dan lugar a un tipo de grietas conocido generalmente con el nombre de "grietas de precalentamiento" que no van a cesar de crecer en el resto de la cocción y que presentan en los productos acabados un aspecto característico.
Resulta muy favorable que los cambios en la estructura física de la pieza sean los mínimos. Por ejemplo que la contracción durante esta fase sea pequeña y que la porosidad resulte también poco aumentada. La variación de estas dos propiedades depende fundamentalmente de la formulación original de la pasta: cuanto menos material arcilloso en la fórmula, menor es la cantidad de agua que se desprende. Cuanto menor el contenido en materia orgánica, menor es el incremento de porosidad producido por su combustión; y cuanto más compacta es la estructura, menores son los movimientos de contracción posibles.
En la zona de temperaturas más elevadas tanto la deformación de las piezas como el crecimiento de las grietas o su reabsorción dependen del acierto tenido al formular la composición en óxidos. En el caso de las pastas interesa que se forme poco líquido y muy bien repartido, es decir, que la composición total establecida esté lejos de los eutécticos posibles a la temperatura de cocción elegida. Normalmente esto se consigue utilizando proporciones de alúmina altas que a su vez tienen la ventaja de permitir contenidos altos de arcilla en la pasta cruda y dar líquidos muy viscosos en estado fundido. Cuando se utilizan temperaturas altas de cocción los altos contenidos en alúmina también proporcionan mayores resistencias mecánicas al posibilitar la formación de mullita.
Bibliografía
- Arcilla y vidriado para el ceramista, Daniel Rhodes. Editorial CEAC, 1990
- Pastas cerámicas, Enrique Gippini. Instituto Eduardo Torroja, 1979
- Ceramic science for the potter, W. G. Lawrence. Chilton Book Company, 1972
- Manual del ceramista, Bernard leach. Editorial Blume, 1981
- The potter's dictionary of materials and techniques, Frank and Janet Hamer. Ed. A&C Black, 2012
- Science for potters, Linda Bloomfield. The American Ceramic Society 2017
- Ceramic Science for the Potter, W. G. Lawrence. First edition, Chilton Book Company, 1972